¿Quieres estar al día? Suscríbete a nuestro newsletter. ¡1 E-mail cada 2 Meses! |
 |
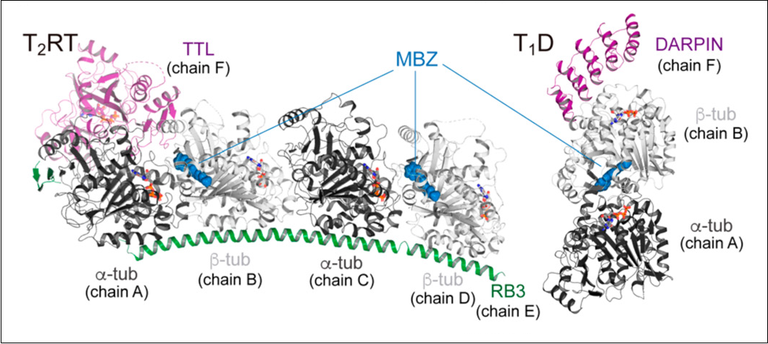
Imagen obtenida en la línea de luz XALOC del ALBA. El fármaco mebendazol (MBZ) se une a la proteína que forma los microtúbulos, la tubulina (T2RT y T1D).
Cerdanyola del Vallès, 5 de mayo 2022 Los microtúbulos son unos filamentos tubulares presentes en el interior de las células. Forman parte de su esqueleto interno e intervienen en el transporte celular. Funcionan como verdaderas carreteras celulares para el transporte de sustancias, vesículas, orgánulos e, incluso, virus, en el caso de que una célula se infecte. De hecho, los virus secuestran esta maquinaria de las células para poder moverse por su interior y replicarse con éxito en su proceso de infección.
La idea es diseñar fármacos que, al unirse a los microtúbulos, impidan que los virus puedan usarlos. En general, los compuestos que atacan a los microtúbulos son llamados MTA (del inglés microtubule targeting agents). Hay dos tipos: los estabilizantes (MSA) y los desestabilizantes (MDA). Hay una larga disponibilidad de ambos y algunos se encuentran en la Lista de Medicamentos Esenciales de la OMS, por lo que son alternativas terapéuticas asequibles y disponibles en todo el mundo.
El equipo del CIB Margarita Salas ha seleccionado 16 MTA comerciales (15 en uso clínico) para estudiar su capacidad de inhibir la replicación viral en 5 virus diferentes: virus del resfriado común (HCoV), el virus responsable de la Covid-19 (SARS-CoV-2), virus de la estomatitis vesicular, el poxvirus vacuna y el virus de la peste porcina africana.
Han confirmado que los MTA afectan la replicación y propagación del virus y que este efecto varía según la dependencia del virus de la red de microtúbulos. "El efecto inhibitorio obtenido varía dependiendo de las funciones específicas que los virus han desarrollado a lo largo de la evolución para explotar la maquinaria de transporte celular de su huésped", explica la Dra. Marian Oliva, miembro del equipo del CIB Margarita Salas-CSIC.
En concreto, los coronavirus CoVs, como el de la Covid-19, tendrían el uso más complejo de los microtúbulos. Estos son necesarios tanto para la internalización del virus en la célula como posteriormente en varios niveles de la formación del sitio de replicación viral. De hecho, las proteínas S y M de los coronavirus (presentes en la superficie del virus) interactúan con la tubulina (proteína de los microtúbulos) durante la infección, aunque actualmente se desconoce cómo lo hacen y qué implicaciones tiene en el desarrollo de la infección; lo que está siendo estudiado en diversos proyectos en marcha que implican la utilización del Sincrotrón ALBA.
"En conjunto hemos confirmado nuestra hipótesis que los microtúbulos son una diana prometedora para el desarrollo de antivirales de amplio espectro. Además, y considerando la gran variedad de efectos según el modelo de virus, necesitamos desarrollar nuevas herramientas de cribado para determinar cuáles son los MTA más adecuados según infecciones virales específicas.", añade la Dra. Oliva.
El equipo de investigación también concluye que los MDA tienen mayor efecto en el transporte intracelular que los MSA, al desestabilizar los microtúbulos e impedir su función de carreteras celulares, bloqueando de esta manera la infección viral. De hecho, un MDA llamado colchicina ha sido usado durante la pandemia de Covid-19 para tratar el síndrome de dificultad respiratoria aguda, dado su conocido efecto antiinflamatorio.
Proteína y fármaco bajo la luz de sincrotrón
Finalmente, otra prueba del efecto antiviral de los MTA fue la obtenida en la línea de luz XALOC del Sincrotrón ALBA. Esta línea ofrece la técnica de difracción de rayos X, mediante la cual se obtiene la imagen tridimensional con alta resolución de la estructura de moléculas. En este caso, el equipo del CIB Margarita Salas-CSIC trajo una muestra de tubulina de mamífero con el fármaco mebendazol, uno de los MTA más eficientes en su trabajo y tomado como representante de la familia de benzimidazoles.
Este complejo proteína-fármaco fue iluminado con los rayos X del sincrotrón y comprobaron, al ver la imagen obtenida tras el posterior tratamiento de datos, dónde se une exactamente el fármaco mebendazol en el complejo de tubulina. Concretamente, en el sitio de la colchicina, bloqueando la proteína e impidiendo que pueda formar el microtúbulo. "El análisis con luz de sincrotrón nos ha permitido saber el mecanismo molecular subyacente del fármaco, lo que contribuye al desarrollo futuro de fármacos específicos para el sitio de unión a la tubulina más eficiente", explica la Dra. Oliva.
Combinando estos diferentes análisis, el equipo científico del CIB Margarita Salas-CSIC ha evidenciado el papel de los MTA en infecciones virales, destacando su actividad como antivirales de amplio espectro, incluso contra la infección por SARS-CoV-2. El Dr. Fernando Díaz matiza que "dada la variedad de procesos en los que los virus pueden secuestrar los microtúbulos, el efecto de los MTA varía según el virus modelo, el tipo de célula y las etapas de infección analizadas. Sin embargo, todos ellos presentan algún grado de efecto antiviral confirmando todavía más que los microtúbulos son una diana clave para la terapia antiviral."
Referencia: María Ángela Oliva, Carlota Tosat-Bitrián, Lucía Barrado-Gil, Francesca Bonato, Inmaculada Galindo, Urtzi Garaigorta, Beatriz Álvarez-Bernad, Rebeca París-Ogáyar, Daniel Lucena-Agell, Juan Francisco Giménez-Abián, Isabel García-Dorival, Jesús Urquiza, Pablo Gastaminza, José Fernando Díaz, Valle Palomo and Covadonga Alonso. Effect of Clinically Used Microtubule Targeting Drugs on Viral Infection and Transport Function. Int. J. Mol. Sci. 2022, 23(7), 3448; https://doi.org/10.3390/ijms23073448
Con la colaboración de la Fundación Española para la Ciencia y la Tecnología. El Sincrotrón ALBA forma parte de la red de Unidades de Cultura Científica y de la Innovación (UCC+i) de la Fundación Española para la Ciencia y la Tecnología (FECYT) y ha recibido apoyo a través del proyecto FCT-20-15798.





